Nukleofile substitutionsreaktioner udgør en hjørnesten inden for organisk kemi. Disse reaktioner er centrale for, hvordan molekyler omformes, idet de muliggør udskiftning af atomer eller funktionelle grupper. I sin essens involverer en nukleofil substitution, at en elektronrig enhed, kendt som en nukleofil, angriber en elektronfattig del af et andet molekyle, ofte kaldet et elektrofil. Resultatet af dette angreb er, at en eksisterende kemisk binding brydes, samtidig med at en ny binding dannes, hvilket fører til, at en del af det oprindelige molekyle udskiftes med nukleofilen.
Forståelsen af nukleofile substitutioner er ikke kun afgørende for teoretisk kemi, men har også vidtrækkende praktiske anvendelser. Fra udviklingen af livsvigtig medicin til fremstillingen af industrielle kemikalier spiller disse reaktioner en kritisk rolle i utallige processer, der påvirker vores hverdag. Selvom princippet lyder simpelt – at bytte en del af et molekyle ud – kan mekanismerne bag disse reaktioner være komplekse og afhænge af en række faktorer, som vi vil udforske nærmere.
- Hvad er en Nukleofil Substitutionsreaktion?
- De To Hovedtyper: SN1 og SN2
- Hvad Betyder Nukleofil?
- Hvad Betyder Elektrofil?
- Sammenligning af SN1 og SN2 Mekanismerne
- Anvendelser og Betydning af Nukleofile Substitutioner
- Substitution vs. Addition
- Konkurrence med Elimination
-
Ofte Stillede Spørgsmål om Nukleofil Substitution
- Hvad er den primære forskel mellem SN1 og SN2 reaktioner?
- Hvad er en nukleofil, og hvordan adskiller den sig fra en elektrofil?
- Hvorfor er nukleofile substitutioner vigtige?
- Hvordan kan man bruge viden om nukleofile substitutioner i en gymnasieopgave?
- Hvad betyder en nukleofils 'hårdhed' eller 'blødhed'?
Hvad er en Nukleofil Substitutionsreaktion?
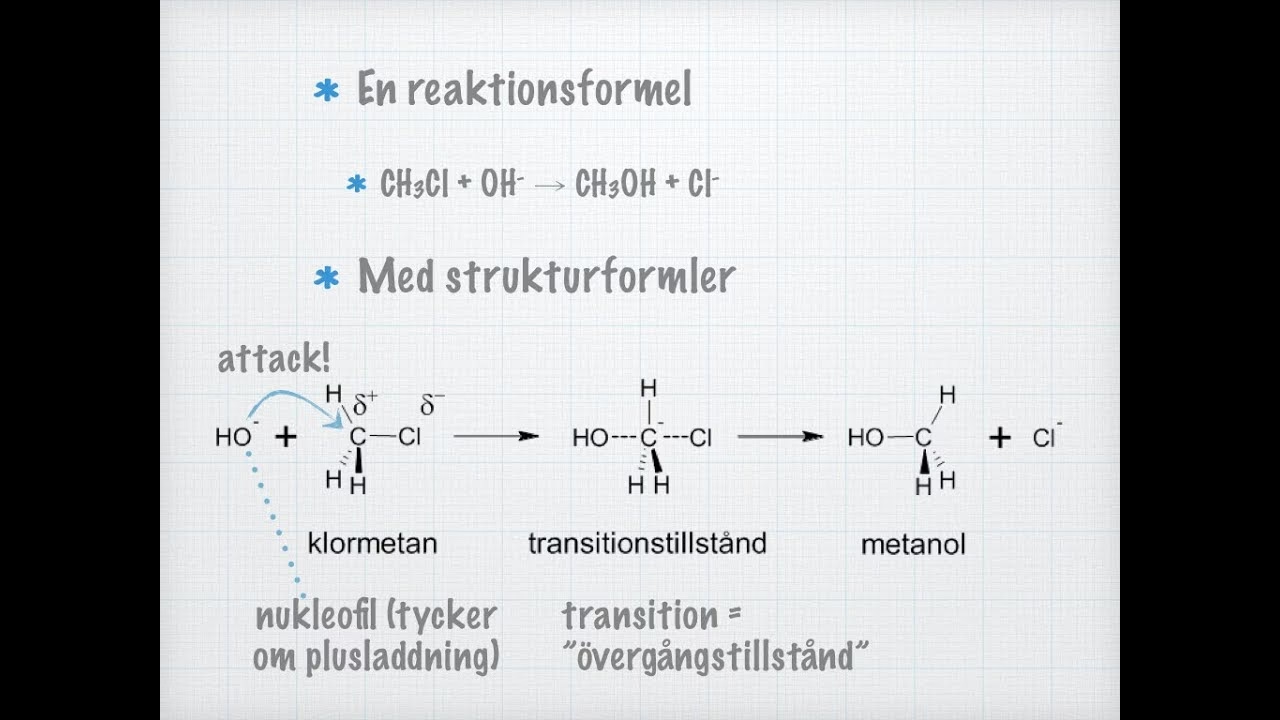
En nukleofil substitutionsreaktion er en kemisk proces, hvor en nukleofil reagerer med et substrat, der indeholder en 'leaving group' (en gruppe, der kan forlade molekylet), og hvor nukleofilen erstatter denne leaving group. Nukleofilen, der er en elektronrig enhed, søger et sted med lav elektrontæthed – et elektrofilt center – for at donere elektroner og danne en ny binding. Substratet i en nukleofil substitution indeholder typisk et kulstofatom, der er bundet til en mere elektronegativ atom (som f.eks. et halogen eller oxygen), hvilket gør kulstofatomet delvist positivt ladet og dermed elektrofilt.
Processen kan beskrives som et 'angreb' fra nukleofilen på det elektrofile center. Dette angreb igangsætter en omlejring af elektroner i substratmolekylet. Den binding, der holder leaving group'en fast til det elektrofile center, svækkes og brydes til sidst, samtidig med at nukleofilen danner en ny binding til det samme center. Resultatet er et nyt produkt, hvor nukleofilen sidder på den position, hvor leaving group'en tidligere sad, og leaving group'en forlader molekylet som en separat enhed, ofte som en anion eller et neutralt molekyle.
Disse reaktioner kræver ofte en vis energitilførsel for at overvinde aktiveringsbarrierer, især for at bryde de eksisterende bindinger. Substitutioner er særligt vigtige reaktioner for visse klasser af organiske forbindelser, herunder alkaner (når de indeholder en passende leaving group) og alkoholer (typisk efter at hydroxylgruppen er omdannet til en bedre leaving group).
De To Hovedtyper: SN1 og SN2
Nukleofile substitutionsreaktioner forekommer primært via to distinkte mekanismer: SN1 og SN2. Forskellen mellem disse mekanismer ligger i, hvordan bindingerne brydes og dannes, og hvor mange molekyler der er involveret i det hastighedsbestemmende trin af reaktionen.
SN1 Reaktioner (Substitution Nucleophilic Unimolecular)
SN1-mekanismen er en to-trins proces. Det afgørende, hastighedsbestemmende trin involverer kun ét molekyle – substratet. I det første trin sker en spontan brud af bindingen mellem det elektrofile kulstofatom og leaving group'en. Dette resulterer i dannelsen af en positivt ladet kulstofart kaldet en carbokation (den 'resulterende positivt ladede ion' nævnt i den indledende forklaring) og frigørelsen af leaving group'en som en anion.
Dannelsen af carbokationen er typisk det langsomste trin i SN1-mekanismen og bestemmer derfor den samlede reaktionshastighed. Jo mere stabil carbokationen er, desto lettere dannes den, og desto hurtigere forløber SN1-reaktionen. Tertiære carbokationer er generelt mere stabile end sekundære, som igen er mere stabile end primære carbokationer. Derfor foretrækkes SN1-mekanismen ofte for substrater, der kan danne stabile carbokationer, såsom tertiære alkylhalider.
I det andet, hurtige trin, angriber nukleofilen den dannede carbokation. Carbokationen har en plan struktur omkring det positive kulstofatom, hvilket betyder, at nukleofilen kan angribe fra begge sider af planet. Dette kan føre til en blanding af produkter, især hvis det elektrofile center oprindeligt var et chiralt center. Man observerer ofte en racemisk blanding af stereoisomerer som produkt af en SN1-reaktion.
SN2 Reaktioner (Substitution Nucleophilic Bimolecular)
SN2-mekanismen er en et-trins, koncerteret proces, hvilket betyder, at bindingen mellem nukleofilen og det elektrofile center dannes samtidigt med, at bindingen mellem det elektrofile center og leaving group'en brydes. Der er ingen mellemtrin som en carbokation i en SN2-reaktion; i stedet passerer reaktionen gennem en overgangstilstand.
I overgangstilstanden er det elektrofile kulstofatom delvist bundet til både den indkommende nukleofil og den udgående leaving group. Overgangstilstanden involverer to molekyler – nukleofilen og substratet – hvilket gør reaktionen bimolekylær. Reaktionen involverer en 'bagside-angreb' af nukleofilen på det elektrofile kulstofatom, modsat placeringen af leaving group'en. Dette angreb forårsager en inversion af konfigurationen omkring det elektrofile kulstofatom, lidt som en paraply, der vender vrangen ud i vinden (kendt som Walden-inversion), hvis kulstofatomet er chiralt.
SN2-reaktioner er stærkt påvirket af sterisk hindring. Nukleofilen skal kunne komme tæt på det elektrofile kulstofatom for at udføre bagside-angrebet. Sterisk hindring omkring dette kulstofatom, forårsaget af store grupper bundet til det, gør overgangstilstanden ustabil og sænker reaktionshastigheden. Derfor foretrækkes SN2-mekanismen for substrater med minimal sterisk hindring omkring det elektrofile center, såsom primære alkylhalider eller methylhalider. Tertiære alkylhalider reagerer stort set ikke via SN2-mekanismen på grund af for stor sterisk hindring.
Hvad Betyder Nukleofil?
Betegnelsen nukleofil stammer fra græsk og betyder 'kerne-elskende'. Dette refererer til, at en nukleofil er tiltrukket af positive ladninger, specifikt de positivt ladede atomkerner (selvom de i kemisk forstand søger regioner med lav elektrontæthed, dvs. elektrofile centre). En nukleofil er en kemisk enhed – et molekyle eller en ion – der er i stand til at donere et elektronpar for at danne en kovalent binding. Dette elektronpar kan enten sidde som en negativ ladning eller som et frit, ikke-bindende elektronpar i en højenergi-orbital på et af atomerne i molekylet.
Nukleofiler er typisk negativt ladede (anioner) eller neutrale molekyler, der indeholder mindst ét atom med et frit elektronpar. Eksempler på nukleofiler inkluderer hydroxid-ionen (OH⁻), alkoxid-ioner (RO⁻), cyanid-ionen (CN⁻), vand (H₂O), alkoholer (ROH), aminer (RNH₂), thioler (RSH) og halogenid-ioner (Cl⁻, Br⁻, I⁻).
Nukleofiler kan klassificeres på flere måder, men to af de vigtigste klassifikationer er baseret på nukleofilicitet og hårdhed/blødhed.
Nukleofilicitet
Nukleofilicitet er et mål for, hvor reaktiv eller 'god' en nukleofil er i en substitutionsreaktion med et standard elektrofil. Det er et kinetisk begreb, der beskriver hastigheden af en nukleofil reaktion. Generelt er der en sammenhæng mellem en nukleofils nukleofilicitet og dens basestyrke: jo stærkere en base (dvs. jo bedre den er til at acceptere en proton), desto bedre er den ofte som nukleofil. Dette skyldes, at både basestyrke og nukleofilicitet afhænger af tilgængeligheden og stabiliteten af elektronparret, der doneres. Dog er der undtagelser, især i forskellige opløsningsmidler, da nukleofilicitet også påvirkes af solvation.
Hårdhed og Blødhed
En nukleofils hårdhed eller blødhed er et udtryk for dens ladningstæthed og polariserbarhed. Dette koncept er en del af HSAB-princippet (Hard and Soft Acids and Bases).
- Hårde nukleofiler: Indeholder typisk små, stærkt elektronegative atomer, der holder deres elektronpar tæt. De har en høj ladningstæthed. Eksempler inkluderer F⁻, OH⁻, H₂O, NH₃. Hårde nukleofiler reagerer primært via elektrostatisk tiltrækning med hårde elektrofiler.
- Bløde nukleofiler: Indeholder typisk store, mindre elektronegative atomer, hvis elektronpar er mere diffust og let polariserbart. De har en lav ladningstæthed over et større volumen. Eksempler inkluderer I⁻, S²⁻, RSH, PR₃. Bløde nukleofiler reagerer primært via kovalent binding og overlapning af orbitaler med bløde elektrofiler.
Forståelsen af en nukleofils hårdhed/blødhed er vigtig, da den påvirker, hvilken type elektrofilt center den foretrækker at reagere med (hårde nukleofiler foretrækker hårde elektrofiler, og bløde nukleofiler foretrækker bløde elektrofiler), og dermed hvilke produkter der dannes, især i reaktioner hvor der er flere mulige reaktionscentre.

Hvad Betyder Elektrofil?
Som modstykket til nukleofilen står elektrofilen. Betegnelsen betyder 'elektron-elskende', og en elektrofil er en enhed, der er i stand til at acceptere et elektronpar for at danne en kovalent binding. Elektrofiler er typisk positivt ladede eller neutrale molekyler med et atom, der har en lav elektrontæthed eller en tom orbital, der kan modtage elektroner.
I nukleofile substitutionsreaktioner er det elektrofile center ofte et kulstofatom, der er bundet til en leaving group, som trækker elektroner væk fra kulstoffet og gør det delvist positivt. Dette gør kulstoffet til et attraktivt mål for den elektronrige nukleofil. Eksempler på elektrofiler ud over de kulstofcentre, der ses i substitutionsreaktioner, inkluderer carbokationer (som i SN1-mekanismen), Lewis-syrer (f.eks. BF₃, AlCl₃) og molekyler med polære dobbelt- eller tripelbindinger (f.eks. carbonylforbindelser).
Sammenligning af SN1 og SN2 Mekanismerne
De to hovedmekanismer, SN1 og SN2, adskiller sig markant i deres forløb, kinetik og stereokemiske udfald. En tabel kan hjælpe med at opsummere de vigtigste forskelle baseret på den information, vi har gennemgået:
| Egenskab | SN1 Reaktion | SN2 Reaktion |
|---|---|---|
| Antal trin | To trin | Ét trin (koncerteret) |
| Hastighedsbestemmende trin | Unimolekylært (afhænger kun af substratkoncentration) | Bimolekylært (afhænger af både substrat- og nukleofilkoncentration) |
| Mellemprodukt | Carbokation (positivt ladet ion) | Ingen stabil mellemprodukt; passerer gennem en overgangstilstand |
| Stereokemi ved chiralt center | Racemisering (blanding af stereoisomerer) | Inversion af konfiguration (Walden-inversion) |
| Foretrækkes af substrater | Tertiære alkylhalider (pga. carbokationstabilitet) | Primære alkylhalider og methylhalider (pga. minimal sterisk hindring) |
| Stærke vs. Svage Nukleofiler | Kræver ikke stærk nukleofil (nukleofilen deltager først i andet trin) | Kræver ofte stærk nukleofil for at drive reaktionen |
Det er vigtigt at bemærke, at valget mellem SN1 og SN2 mekanisme ikke altid er entydigt og kan påvirkes af andre faktorer som opløsningsmiddeltype (polære protiske opløsningsmidler favoriserer SN1, polære aprotiske opløsningsmidler favoriserer SN2) og den specifikt involverede leaving group.
Anvendelser og Betydning af Nukleofile Substitutioner
Nukleofile substitutionsreaktioner er ikke kun et akademisk emne; de er af fundamental betydning på tværs af mange grene af kemien og beslægtede videnskaber.
- Organisk Syntese: I organisk syntese er nukleofile substitutioner uundværlige værktøjer til at opbygge komplekse molekyler. De giver kemikere mulighed for at introducere en bred vifte af funktionelle grupper på specifikke positioner i et molekyle. Ved at vælge det passende substrat, nukleofil og reaktionsbetingelser kan man styre, hvilken type substitution der finder sted (SN1 eller SN2) og dermed opnå det ønskede produkt med høj selektivitet. Denne evne til præcist at modificere molekylære strukturer er kernen i syntetisk kemi.
- Medicinsk Kemi og Farmaci: Inden for medicinsk kemi er design og syntese af lægemidler ofte stærkt afhængig af nukleofile substitutioner. Mange lægemidler indeholder specifikke funktionelle grupper, der indføres eller modificeres ved hjælp af disse reaktioner. For eksempel kan syntesen af antibiotika, antivirale midler eller kræftmedicin involvere nøje kontrollerede nukleofile substitutionstrin for at skabe molekyler med de ønskede biologiske egenskaber.
- Biokemi: Selv i levende organismer forekommer nukleofile substitutionsreaktioner. Enzymatiske reaktioner, der katalyserer dannelsen eller nedbrydningen af biologisk aktive forbindelser, kan involvere nukleofile angreb. For eksempel kan overførsel af en phosphatgruppe i energimetabolismen eller modifikation af proteiner involvere mekanismer, der ligner nukleofil substitution.
- Industrielle Processer: Produktionen af mange kemiske forbindelser i stor skala i industrien udnytter nukleofile substitutioner. Dette inkluderer fremstilling af polymerer, opløsningsmidler, pesticider og andre finkemikalier. Effektiv og selektiv udførelse af disse reaktioner er afgørende for at minimere affald og maksimere udbyttet i industriel skala.
- Miljøpåvirkninger: Nukleofile substitutioner spiller også en rolle i miljøkemien. For eksempel kan nedbrydningen af visse forurenende stoffer i miljøet ske via nukleofile reaktioner, ofte med vand som nukleofil (hydrolyse). Forståelse af disse reaktionsveje er vigtig for at vurdere persistensen og skæbnen for kemikalier i miljøet og for at udvikle strategier til oprydning af forurening.
- Analytisk Kemi: I analytisk kemi kan nukleofile substitutioner anvendes til at modificere forbindelser for at gøre dem lettere at detektere eller kvantificere. Der findes også analytiske metoder, der specifikt udnytter nukleofile reaktioners principper til identifikation eller analyse af kemiske stoffer.
Disse eksempler understreger, at nukleofile substitutioner er mere end blot et teoretisk koncept; de er fundamentale processer med bred anvendelse og stor betydning for mange områder af videnskab og teknologi.
Substitution vs. Addition
Det er nyttigt at differentiere substitutionsreaktioner fra andre typer reaktioner, især additionsreaktioner, som er et andet almindeligt reaktionsmønster i organisk kemi. Som nævnt bytter atomer eller molekyledele plads i en substitutionsreaktion. Dette sker typisk på et mættet kulstofatom (et kulstofatom, der kun er bundet til fire andre atomer via enkeltbindinger) eller på et aromatisk system.
I en additionsreaktion sættes to molekyler sammen for at danne et større molekyle. Dette sker typisk ved, at en dobbelt- eller tripelbinding i et umættet molekyle brydes, og nye enkeltbindinger dannes til atomerne fra det andet molekyle. Der er altså ingen 'leaving group', der forlader molekylet; i stedet 'adderes' noget til molekylet ved at mætte en dobbelt- eller tripelbinding.
Mens begge reaktionstyper involverer dannelse og brud af kovalente bindinger, er det fundamentale princip bag dem forskelligt: substitution handler om udskiftning på et eksisterende 'skelet', mens addition handler om at 'lægge til' et umættet 'skelet'.
Konkurrence med Elimination
I mange tilfælde, hvor en nukleofil substitution er mulig, er en anden type reaktion kaldet elimination også mulig. Elimination er en proces, hvor atomer eller grupper fjernes fra et molekyle, ofte for at danne en dobbelt- eller tripelbinding. Ligesom nukleofil substitution kan elimination forekomme via forskellige mekanismer, herunder E1 og E2, som ofte konkurrerer med henholdsvis SN1 og SN2.
For eksempel, når en nukleofil (der også kan fungere som en base) reagerer med et alkylhalid, kan den enten angribe det elektrofile kulstofatom og forårsage substitution, eller den kan angribe en proton på et nabokulstofatom og forårsage elimination af både protonen og leaving group'en, hvilket resulterer i dannelsen af en alken. Betingelserne for reaktionen, såsom basens/nukleofilens styrke, opløsningsmidlet og temperaturen, spiller en afgørende rolle for, hvilken reaktion – substitution eller elimination – der foretrækkes. En stærk, sterisk hindret base/nukleofil i et protisk opløsningsmiddel ved høj temperatur vil ofte favorisere elimination, mens en stærk, lille nukleofil i et aprotisk opløsningsmiddel ved lav temperatur vil favorisere SN2 substitution (givet et passende substrat).
Ofte Stillede Spørgsmål om Nukleofil Substitution
Her besvarer vi nogle almindelige spørgsmål relateret til nukleofile substitutioner:
Hvad er den primære forskel mellem SN1 og SN2 reaktioner?
Hovedforskellen ligger i mekanismen. SN1 er en to-trins proces med dannelse af en carbokation som mellemprodukt, mens SN2 er en et-trins koncerteret proces uden stabilt mellemprodukt, men med en overgangstilstand. SN1 er unimolekylær i det hastighedsbestemmende trin, mens SN2 er bimolekylær.
Hvad er en nukleofil, og hvordan adskiller den sig fra en elektrofil?
En nukleofil er en elektronrig enhed (molekyle eller ion), der donerer et elektronpar. En elektrofil er en elektronfattig enhed, der accepterer et elektronpar. Nukleofilen angriber elektrofilen.
Hvorfor er nukleofile substitutioner vigtige?
De er fundamentale i organisk syntese for at bygge og modificere molekyler. De er afgørende i medicinsk kemi til syntese af lægemidler, i industrien til kemisk produktion, i biokemi for enzymatiske processer og i miljøkemi for nedbrydning af stoffer.
Hvordan kan man bruge viden om nukleofile substitutioner i en gymnasieopgave?
Du kan forklare reaktionsmekanismerne (SN1/SN2), diskutere deres anvendelse i organisk syntese (f.eks. alkylhalider), undersøge deres relevans i biokemi eller farmaceutisk kemi, analysere deres miljøpåvirkninger, eller sammenligne dem med konkurrerende reaktioner som elimination (E1/E2). Du kan også dykke ned i, hvordan faktorer som substratstruktur, nukleofilens styrke/størrelse og opløsningsmiddel påvirker reaktionsvejen.
Hvad betyder en nukleofils 'hårdhed' eller 'blødhed'?
Det beskriver ladningstætheden og polariserbarheden af nukleofilen. Hårde nukleofiler har høj ladningstæthed og reagerer elektrostatisk, mens bløde nukleofiler har lav, diffus ladningstæthed og reagerer via orbitaloverlap. Dette påvirker, hvilken type elektrofil de foretrækker at reagere med.
Forståelsen af nukleofile substitutioner er essentiel for enhver, der studerer eller arbejder med organisk kemi. De er alsidige reaktioner, der ligger til grund for utallige transformationer og processer i både laboratoriet og naturen.
Hvis du vil læse andre artikler, der ligner Nukleofil Substitution: En Dybdegående Guide, kan du besøge kategorien Fotografi.
